阿尔茨海默病(AD)导致的记忆和自我意识的缓慢丧失,是现代医学面临的最严峻挑战之一。当我们眼睁睁地看着挚爱之人逐渐失去认知能力时,传统疗法的局限性便显露无疑。然而,新兴研究表明,我们或许正接近一个转折点,再生医学不仅能缓解症状,更有可能改写疾病的进程。.
了解阿尔茨海默病概况
阿尔茨海默病并非仅仅是“健忘”。这种神经退行性疾病会逐渐破坏神经元,其病理特征是β-淀粉样蛋白斑块和神经原纤维缠结。突触紊乱会导致记忆力衰退、意识混乱、性格改变,并最终导致身体机能丧失。目前美国食品药品监督管理局(FDA)批准的药物——乙酰胆碱酯酶抑制剂和NMDA受体拮抗剂——只能在一定程度上延缓症状,但无法阻止神经退行性变。这种治疗上的困境促使人们探索再生疗法。.
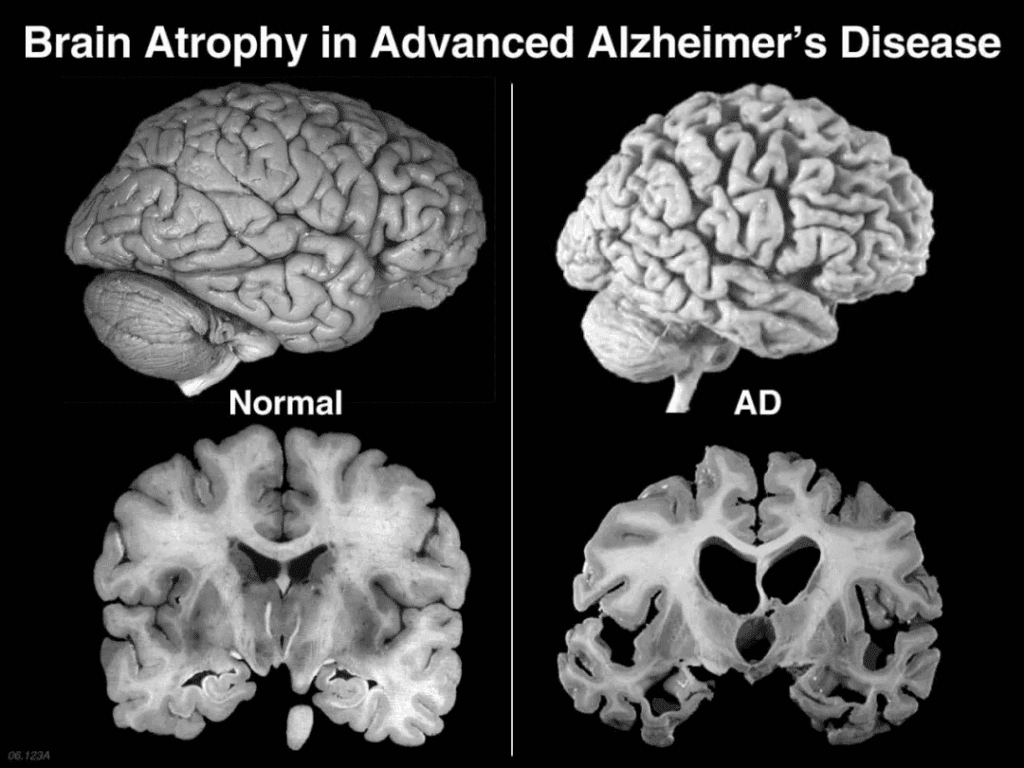
脑损伤是阿尔茨海默病的原因。
hUC-MSCs:不仅仅是简单的细胞替代
人类脐带 脐带间充质干细胞(hUC-MSCs)具有独特的生物学特性,使其成为极具潜力的阿尔茨海默病(AD)治疗药物。与胚胎干细胞不同,这些来源符合伦理规范的细胞具有低免疫原性和强大的免疫调节功能。它们的治疗机制不仅限于神经元替代:
旁分泌信号传导: hUC-MSCs 分泌神经营养因子(BDNF、GDNF),可挽救受损神经元并刺激突触再生。.
小胶质细胞调节: 它们通过将破坏性小胶质细胞转化为神经保护表型来抑制神经炎症。.
淀粉样蛋白清除: 通过增强吞噬作用和酶促降解(脑啡肽酶上调)。.
值得注意的是,2022 年 干细胞 研究与治疗 研究表明,在 AD 小鼠体内静脉注射 hUC-MSCs 可减少 40% 淀粉样蛋白负荷,并通过选择性地归巢到发炎的大脑区域来改善认知评分——这是一种我们才刚刚开始了解的生物“分诊”系统。.
CRISPR:用于神经退行性疾病的精准工程
 尽管 干细胞 CRISPR-Cas9基因编辑技术提供了生物“硬件”,而CRISPR-Cas9则提供了“软件”升级。这种分子手术刀能够在移植前对干细胞中与疾病相关的基因进行精确修饰。在阿尔茨海默病(AD)的治疗中,CRISPR增强型疗法包括:
尽管 干细胞 CRISPR-Cas9基因编辑技术提供了生物“硬件”,而CRISPR-Cas9则提供了“软件”升级。这种分子手术刀能够在移植前对干细胞中与疾病相关的基因进行精确修饰。在阿尔茨海默病(AD)的治疗中,CRISPR增强型疗法包括:
- APOE4 更正: 将高风险的ε4等位基因转化为具有神经保护作用的ε3变体
- BACE1基因敲除: 通过靶向β-分泌酶基因来减少淀粉样蛋白的形成过程
- 神经营养增强剂: 插入基因以增强 BDNF 或 NGF 的产生
2023 年一项具有突破性意义的研究表明 自然神经科学 将 CRISPR 编辑的间充质干细胞与纳米颗粒递送相结合,在灵长类动物模型中实现了比未修饰细胞高 68% 倍的淀粉样蛋白清除率。这种协同作用体现了工程化细胞如何成为大脑内的靶向药物工厂。.
风暴将至——以及前进的道路
据预测,到2050年,全球阿尔茨海默病病例将增加两倍,达到1.52亿例(国际阿尔茨海默病协会,2023),形势紧迫。近期临床进展凸显了其潜力:
I/II期临床试验(NCT03172117,NCT02600130)显示,人脐带间充质干细胞(hUC-MSC)输注可显著改善轻度至中度阿尔茨海默病患者的简易精神状态检查量表(MMSE)评分,且疗效可持续至治疗后12个月以上。正电子发射断层扫描(PET)成像显示,关键记忆区域的淀粉样蛋白沉积减少,代谢活性得以维持。.
然而,挑战依然存在——优化递送方法、防止细胞衰老以及确保长期安全性。目前最有前景的研究集中在联合疗法上:通过鼻内途径递送经 CRISPR 增强的干细胞以绕过血脑屏障,并可能与抗 tau 蛋白生物制剂联合使用。.
当我们站在这个跨学科的十字路口时,再生策略带来的不仅仅是渐进式的进步。它们代表着从应对衰退到重建神经完整性的根本性转变。虽然目前还不是万能药,但干细胞生物学和精准技术的融合正在带来巨大的希望。 基因编辑 这带来了切实的希望,我们或许有一天能将阿尔茨海默病从绝症转变为可治疗的疾病——不仅能保存记忆,还能保存身份。.
参考: 国际阿尔茨海默病协会 (2023)。世界阿尔茨海默病报告。| Kim 等 (2022)。干细胞研究与治疗。13(1):489。| Liu 等 (2023)。自然神经科学。26(5):765-778。| ClinicalTrials.gov 标识符:NCT03172117、NCT02600130。.


