干细胞与其他细胞的区别是我在医学研究中最引人入胜的过程之一。这些“万能细胞”是人体内唯一能够分化成200多种不同类型特化细胞的细胞。它们非常神奇——与寿命有限的普通细胞不同,干细胞能够不断更新并复制自身。.
干细胞是构成我们身体的基本单元。人体利用它们作为天然的修复系统。造血干细胞维持血液和免疫细胞的生成,而 间充质干细胞 细胞支撑着骨骼、软骨、肌肉和脂肪。我最喜欢这些细胞的一点是它们具有分化成不同类型细胞的能力——从血细胞到神经细胞再到心肌细胞。这使得它们成为获取医学研究和治疗见解的绝佳途径。.
干 细胞疗法 这些细胞疗法在治疗各种疾病方面展现出巨大潜力。这一点至关重要,因为约有 60% 的美国成年人患有慢性疾病,这表明人们对新的治疗方法有着迫切的需求。慢性疾病的种类还在不断增加——从关节炎和多发性硬化症到各种癌症和心脏病。当常规疗法无效时,这些细胞疗法带来了新的希望。.
本文将深入探讨细胞重编程的科学原理,以及科学家如何利用干细胞改变医学。我们将研究驱动细胞发育的机制、引导细胞生长的最快方法,以及正在改善患者护理的令人振奋的临床应用。.
干细胞分化的分子基础
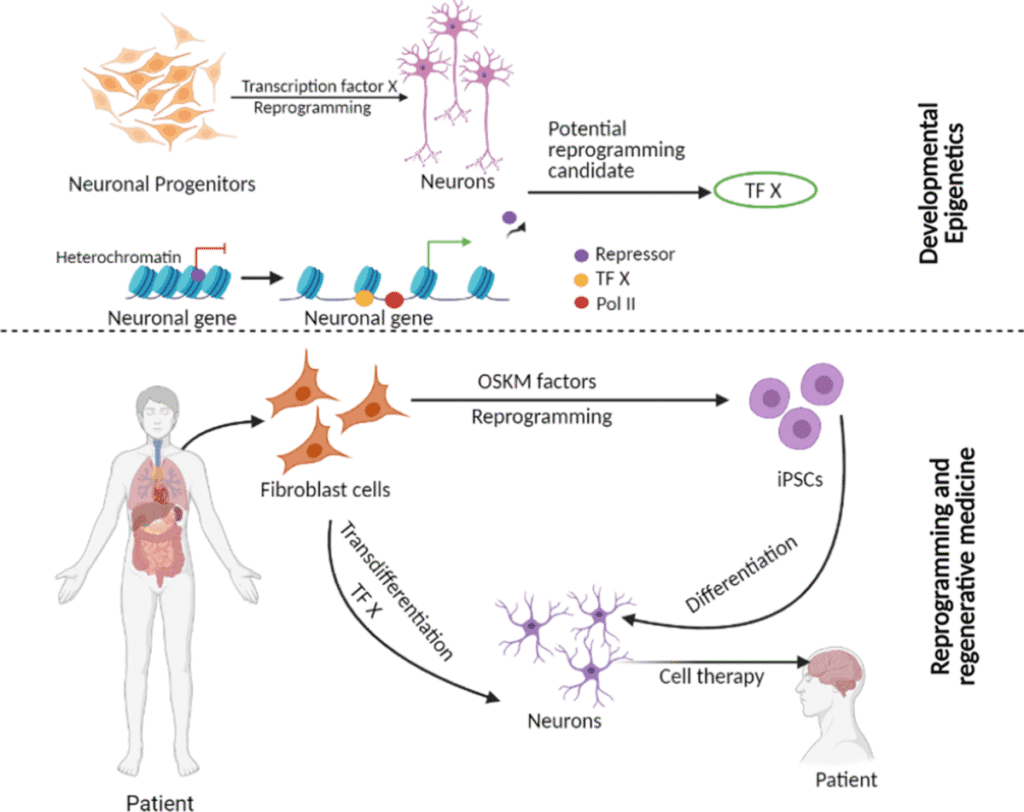
图片来源: 临床表观遗传学 – 生物医学中心
干细胞分离的分子复杂性取决于精细的遗传和表观遗传机制,这些机制将未分化的细胞转化为功能性的、组织特异性的细胞。科学家们现在认为,理解这些机制对于推进再生医学的发展至关重要。.
多能性与多重潜能:主要区别
干细胞的分离能力决定了其细胞分化潜能。多能干细胞 干细胞 多能干细胞(PSCs)可以分化成来自所有三个胚层——外胚层、中胚层和内胚层的细胞。这些细胞不能形成胎盘或脐带等胚外组织。多能干细胞只能分化成特定谱系内密切相关的细胞类型。造血干细胞(HSCs)专门产生各种血细胞,而间充质干细胞(MSCs)则可分化成骨细胞、软骨细胞、肌肉细胞和脂肪细胞。这种分化潜能的根本差异决定了每种干细胞类型可以治疗哪些疾病。.
谱系定向中的转录因子
转录因子(TFs)在干细胞分离过程中发挥着关键调控作用。多能干细胞的核心转录因子包括OCT4、SOX2和NANOG,它们维持着干细胞的自我更新能力。这些因子通过与特定的DNA序列结合,调控维持干细胞特性所必需的基因表达。.
不同的转录因子在谱系分化过程中决定细胞命运。例如:
- RUNX2 和 Osterix 引导间充质干细胞向骨形成方向发展
- PPARγ 指导脂肪生成
- SOX9 控制软骨细胞分化
- GATA-1、GATA-2 和 PU.1 调控造血发育
研究表明,即使激活单个谱系特异性转录因子,也能将祖细胞转化为不同的谱系。.
分化过程中的表观遗传调控
表观遗传机制对干细胞命运的影响远超转录因子。DNA甲基化、组蛋白修饰和非编码RNA调控构成了这些机制。.
与自我更新相关的基因逐渐沉默,而谱系特异性基因在分化过程中被激活。CpG位点DNA甲基化模式的动态变化和组蛋白的修饰驱动着这一过程。组蛋白H3K4的甲基化激活基因,而H3K27的甲基化则使其沉默。具有相反活性的染色质修饰酶实现了细胞重编程所需的精确且可逆的调控。.
细胞重编程和诱导多能干细胞(iPSCs)
细胞重编程彻底改变了我们对细胞命运可塑性的理解,并为再生医学开辟了新的可能性。本节将深入探讨如何通过基因操作使分化细胞逆转为多能干细胞状态。.
山中因子和iPSC生成
山中伸弥和高桥和俊在2006年取得了突破性进展,他们将小鼠成纤维细胞重编程为诱导多能干细胞。 干细胞他们发现了四种关键的转录因子——Oct3/4、Sox2、Klf4 和 c-Myc——现在被称为山中因子,这些因子可以将体细胞转化为多能干细胞。2007 年,他们成功地利用成人真皮成纤维细胞实现了这一目标。 .
这些山中因子触发维持多能性的关键发育信号通路。具体而言:
- Oct4 和 Sox2 在调控发育过程中发挥着核心作用。
- Klf4 改善了 Oct4 和 Sox2 的活动
- c-Myc在代谢过程中发挥着独特的作用
体细胞核移植与诱导多能干细胞重编程
核重编程主要通过两种方法实现:体细胞核移植(SCNT)和诱导多能干细胞(iPSC)生成。SCNT利用未受精卵的细胞质将体细胞基因组重编程为全能状态,这是最彻底的表观遗传重编程过程。iPSC技术则采用不同的方法,通过暂时过表达转录因子来重置体细胞,而无需使用人类卵子。.
两种方法都能制备患者特异性的多能干细胞。体细胞核移植(SCNT)在多种脊椎动物中效果良好,但面临技术、法律和伦理方面的挑战。诱导多能干细胞(iPSC)重编程技术虽然操作更简便,但效率和速度远不及SCNT。.
重编程细胞遗传不稳定性风险
诱导多能干细胞(iPSCs)展现出应用前景,但也引发了人们对其基因组完整性的担忧。比较基因组杂交分析显示,重编程细胞中存在缺失和扩增。这些特征表明,癌基因诱导了DNA复制应激。基因组变化很大程度上取决于c-Myc的表达。.
该方法效率较低(约0.01–0.1%),表明该技术存在问题。当科学家阻断p53等抑癌基因时,p53通路受损的细胞更容易被重编程。早期传代的iPSCs也比中期传代细胞或成纤维细胞含有更多的拷贝数变异。.
材料与方法:培养和引导分化
科学家需要精确控制细胞环境才能有效地诱导干细胞分化。过去几年里,研究团队开发了更先进的方法来培养和引导这些多功能细胞的发育。.
用于多能干细胞的无饲养层培养系统
小鼠胚胎成纤维细胞 (MEF) 是传统干细胞培养的基础。这些细胞分泌重要的生长因子,例如 TGFβ、激活素 A 和细胞外基质。科学家们利用 Matrigel 开发了无需饲养层的替代培养方法。Matrigel 含有层粘连蛋白、IV 型胶原蛋白和硫酸肝素蛋白聚糖。Matrigel 可通过特定的培养基配方支持干细胞生长,是首批替代饲养层依赖型培养方法的方案之一。然而,由于其来源于小鼠肉瘤,因此存在异种污染的风险。.
科学家们开发了更明确的底物,包括特定的层粘连蛋白亚型(-511/-521)、玻连蛋白和E-钙黏蛋白。基于合成聚合物的平台,例如PMEDSAH和氨丙基甲基丙烯酰胺(APMAAm)等两性离子水凝胶,提高了实验的重复性。石墨烯基表面有望在无需细胞外基质包被的情况下维持细胞的多能性。.
定向分化的生长因子方案
科学家将细胞暴露于特定的生长因子中,这些生长因子模拟发育信号,从而引导干细胞分化。基本实验方案始于以下任一步骤:
- 悬浮培养中通过细胞聚集形成胚状体(EB)
- 单层细胞分化与连续生长因子暴露
特定的生长因子组合引导谱系特异性发育。神经分化需要bFGF、肝素和N2补充剂。10日龄胚状体自然分化为心脏细胞,而激活素A则驱动内胚层诱导。BMP-4、TGF-β1、维甲酸和HGF通过激活不同的信号通路引导细胞走向特定的命运。 .
用于组织特异性发育的3D类器官模型
科学家们已经超越了简单的细胞分化,创造出能够模拟组织结构的复杂三维类器官模型。干细胞在三维基质的支持下,通过其自组织能力形成类器官。这些结构比传统培养方法能够形成更复杂的形态,并提供更好的组织发育模型。.
科学家首先将干细胞嵌入水凝胶(例如 Matrigel、藻酸盐或合成聚乙二醇 (PEG) 基质)中,以此构建类器官。基质的物理特性与提供必需营养物质的生物反应器相结合,能够促进类器官的发育。这种方法已成功构建了肠道、大脑、肾脏和肝脏的类器官模型,为疾病建模和药物筛选提供了极佳的参考。 .
结果与讨论:分化干细胞的临床应用
过去几年,科学家们已将干细胞疗法的理论可能性转化为实际疗法。他们严谨的研究和临床试验如今能够帮助治疗以前无法治愈的疾病。.
利用iPSC衍生心肌细胞进行心脏修复
诱导多能干细胞来源的心肌细胞(iPSC-CMs)在治疗心力衰竭和心肌梗死方面展现出显著的潜力。将这些细胞移植到受损心脏后,与对照组相比,左心室射血分数提高了8.23%。心脏功能在治疗后4-8周内改善最为显著,但此后疗效逐渐下降。.
对非人灵长类动物的研究表明,将诱导多能干细胞来源的心肌细胞与内皮细胞结合,可以促进缺血再灌注后移植组织的增大、血管形成和心脏功能。这些改善源于受损组织的再肌肉化和移植组织内更好的血管化。 .
帕金森病模型中的神经再生
诱导多能干细胞(iPSC)衍生的神经干细胞(NSC)在治疗帕金森病方面展现出巨大的潜力。 细胞可以 转化为多巴胺能神经元——帕金森病中主要丢失的细胞类型。移植的细胞能够存活,并通过分泌多巴胺和提供营养支持来帮助治疗。.
临床试验证实神经干细胞移植安全有效,并能改善帕金森病患者的运动功能。敲低SNCA基因的人类诱导多能干细胞来源的神经干细胞能够改善小鼠模型的协调性、平衡性和运动能力,并延长小鼠的寿命。 .
临床试验中干细胞治疗的疾病列表
目前,干细胞疗法已应用于临床试验,用于治疗多种疾病:
- 血液疾病白血病、淋巴瘤、多发性骨髓瘤
- 神经系统疾病帕金森病、阿尔茨海默病、肌萎缩侧索硬化症
- 心血管疾病心力衰竭、心肌梗塞
- 免疫系统疾病多发性硬化症、1型糖尿病
- 其他条件骨关节炎、克罗恩病引起的肛周瘘管
几十年来,医生们一直成功地运用造血干细胞移植(骨髓移植)来治疗血液相关癌症。当常规治疗效果不佳时,干细胞移植是一种有效的治疗方法。然而,在广泛应用之前,我们还需要进行更多的研究。.
结论
本文探讨了干细胞从未分化状态到具有特定功能的特化细胞的奇妙旅程。驱动分化的分子机制——从OCT4和SOX2等转录因子到复杂的表观遗传修饰——揭示了指导细胞发育的复杂生物学程序。科学家们证明,通过山中因子,成体细胞可以被重编程回多能干细胞状态,这无疑彻底改变了我们对干细胞的理解。然而,这一过程在遗传稳定性方面仍然面临挑战。.
科学家们通过先进的培养技术重塑了干细胞研究格局。他们现在使用复杂的系统,并已从简单的饲养层发展到使用特定的基质。能够更好地模拟天然组织环境的复杂三维类器官模型,使得对分化途径的控制更加精准,并能更有效地模拟人类疾病。.
分化干细胞的临床应用正迅速扩展。这些疗法为医生们曾经认为无法治愈的疾病带来了希望,从心脏组织再生到帕金森病的神经细胞移植。许多应用仍处于实验阶段,但造血干细胞移植等成功的治疗方法展现了其真正的潜力。.
该领域未来必须克服诸多挑战。科学家需要提高分化效率、确保遗传稳定性并扩大生产规模以满足临床应用需求。细胞重编程背后的科学正在不断进步,干细胞疗法将成为现代医学的关键组成部分。这些疗法将为全球患者提供个性化的治疗方案。从实验室研究到临床应用的整个过程,展现了基础生物学研究如何重塑临床实践并改变人类生活。.


